Le point sur le bévacizumab dans les gliomes de haut grade

Par M. Bruno Chauffert dijon
Par Bruno Chauffert (CHU d'Amiens)Les gliomes de haut grade (GHG) sont des tumeurs hypervascularisées avec une rupture locale de la barrière hémato-cérébrale responsable d’une prise de contraste intense en IRM. Le bévacizumab (BVZ) est le seul anticorps monoclonal humanisé disponible qui cible la néo-angiogenèse tumorale, par le biais de la déplétion du VEGF A circulant.
L’activité du BVZ sur les GHG récidivant après le classique schéma témozolomide/radiothérapie a été mise en évidence par Stark-Vance et coll. en 2005 et confirmée par Vredenburgh et coll. en 2007. Il a été montré que le BVZ seul, à la dose de 10 mg/kg toutes les 2 semaines, était aussi efficace que l’association irinotécan/BVZ utilisée dans les premières études (Friedman et coll.).
L’activité du BVZ n’est pas potentialisée par l’association à des médicaments cytotoxiques. Il faut aussi souligner l’absence d’efficacité des autres anti-angiogéniques par voie orale, et en général des molécules ciblant les tyrosine-kinases.
Plus de la moitié des patients bénéficient d’une amélioration clinique rapide, avec une diminution concomitante de la prise de contraste en imagerie. Le BVZ a un effet marqué contre l’œdème cérébral et permet d’épargner les corticoïdes. La tolérance est assez bonne même s’il faut connaître le risque d’hémorragie cérébrale (de 2 à 4% des patients), d’une majoration ou de l’apparition d’une hypertension artérielle (environ 30% des cas) facilement contrôlable en général par une majoration du traitement, et d’événements thrombo-emboliques veineux (environ 30% des cas) qui ne contrindiquent pas la poursuite du BVZ en association avec les héparines de bas poids moléculaire.
Un syndrome néphrotique peut survenir (moins de 5% des patients) car le VEGF A est nécessaire à l’intégrité de la membrane basale glomérulaire ; une surveillance régulière de la protéinurie est recommandée.
La survie sans progression supérieure (PFS) est de l’ordre de 40% à 6 mois et de l’ordre de 10% à 12 mois, ce qui est remarquable dans la situation de récidive d’un GHG. Cette efficacité, confirmée par de nombreuses études dont celle de l’ANOCEF (Guiu et coll.), a suscité beaucoup d’espoir dans un domaine où la ressource thérapeutique reste faible. Le BVZ a bénéficié d’un enregistrement accéléré par la FDA américaine (x) malgré un développement industriel atypique, et notamment l’absence d’étude de phase III montrant un bénéfice en survie globale.
L’Agence Européenne du Médicament (EMA) a créé la surprise en 2009 en ne recommandant pas le BVZ tant qu’une étude de phase III ne serait pas disponible. L’EORTC est chargée de conduire cette étude qui randomise actuellement BVZ contre lomustine, une nitrosourée considérée comme le traitement standard, même si son activité est limitée (PFS 1,6 mois). Au moins trois études randomisées, dont une de l’ANOCEF (AVAGLIO, RTOG, TEMAVIR) sont en cours pour évaluer l’apport du BVZ en première ligne, en association avec le traitement standard par radiothérapie et témozolomide.
Malgré le moratoire de l’EMA, de nombreux neuro-oncologues français utilisent le BVZ en situation de récidive. Une étude de cohorte, menée par Taillibert et coll. collige ces observations et sera bientôt publiée. Les autorités de régulation française (INCA, Sécurité Sociale) ont laissé pour l’instant la liberté d’un usage compassionnel jusqu’au résultat des études en cours.
Au total, même s’il n’est pas le traitement curatif qu’on attend encore, le BVZ est un médicament majeur en neuro-oncologie dont la place mérite d’être mieux définie par le biais des études cliniques, d’autant qu’il est cher (de l’ordre de 4000€ par mois, soit autant que le coût d’une dialyse chronique). L’effet rapide du BVZ sur les symptômes cliniques (hypertension intracrânienne, déficit neurologique) pourrait être exploité chez les patients dont l’état général et neurologique initial ne permet pas immédiatement la réalisation d’une radiochimiothérapie standard. Une demande de PHRC a été déposée au nom de l’ANOCEF pour étudier l’introduction précoce de l’association bévacizumab/temozolomide avant la radiochimiothérapie.
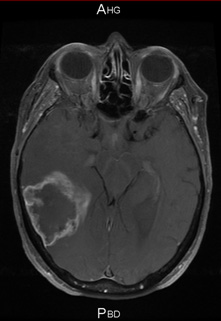
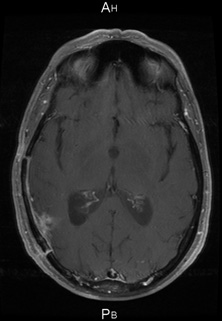
Mars 2011 Juin 2011
Mars 2011 : Patiente de 59 ans porteuse d’un glioblastome avec hémiplégie gauche ne permettant plus la marche.
D’avril 2011 à juin 2011 : bévacizumab 10 mg/kg en IV tous les 15 jours et témozolomide (150 puis 200 mg/m2/jour x 5 jours) à 4 semaines d’intervalle.
Récupération complète de l’hémiplégie.
Juillet/août 2011 : Radiochimiothérapie selon ‘’Stupp’’ en poursuivant le BVZ pendant la radiothérapie
Octobre 2011. Aucun déficit neurologique. OMS 0. Temozolomide adjuvant en cours et bévacizumab tous les 15 jours.
Références :
Cloughesy T. FDA accelerated approval benefits glioblastoma. Lancet Oncol. 2010;11(12):1120.
►Retrouvez l’abstract en ligne
Friedman HS, Prados MD, Wen PY et al. Bevacizumab alone and in combination with irinotecan in recurrent glioblastoma. J Clin Oncol. 2009;27(28):4733-40.
►Retrouvez l’abstract en ligne
Guiu S, Taillibert S, Chinot O et al. Bevacizumab/irinotecan. An active treatment for recurrent high grade gliomas: preliminary results of an ANOCEF Multicenter Study. Rev Neurol (Paris). 2008;164(6-7):588-94.
►Retrouvez l’abstract en ligne
Stark-Vance V. Bevacizumab and CPT-11 in the treatment of relapsed malignant glioma. In: World Federation of Neuro-Oncology Meeting; 2005 May; 2005. p. 91.
Vredenburgh JJ, Desjardins A, Herndon JE 2nd et al. Bevacizumab plus irinotecan in recurrent glioblastoma multiforme. J Clin Oncol. 2007;25(30):4722-9.
►Retrouvez l’abstract en ligne
Wick W, Puduvalli VK, Chamberlain MC et al. Phase III study of enzastaurin compared with lomustine in the treatment of recurrent intracranial glioblastoma. J Clin Oncol. 2010;28(7):1168-74.
►Retrouvez l’abstract en ligne
Date de publication : 1er décembre 2011





